730. Prečo sa voda používa na chladenie niektorých mechanizmov?
Voda má skvelú špecifické teplo, čo prispieva k dobrému odvodu tepla z mechanizmu.
731. V akom prípade treba vynaložiť viac energie: na zohriatie jedného litra vody o 1 °C alebo na zohriatie sto gramov vody o 1 °C?
Na zahriatie litra vody, pretože čím väčšia je hmotnosť, tým viac energie je potrebné minúť.
732. Kupronickel a strieborné vidličky rovnakej hmotnosti sa ponorili do horúcej vody. Prijímajú rovnaké množstvo tepla z vody?
Kuproniklová vidlica dostane viac tepla, pretože špecifické teplo kupronického niklu je väčšie ako striebra.
733. Kus olova a kus liatiny rovnakej hmotnosti bol trikrát udieraný perlíkom. Ktorá časť bola teplejšia?
Olovo sa zahreje viac, pretože jeho špecifická tepelná kapacita je menšia ako u liatiny a na ohrev olova je potrebných menej energie.
734. Jedna banka obsahuje vodu, druhá obsahuje petrolej rovnakej hmotnosti a teploty. Do každej banky sa hodila rovnako zahriata železná kocka. Čo sa viac zahreje vysoká teplota- voda alebo petrolej?
Petrolej.
735. Prečo sú teplotné výkyvy v zime a v lete v mestách na pobreží menej prudké ako v mestách vo vnútrozemí?
Voda sa ohrieva a ochladzuje pomalšie ako vzduch. V zime sa ochladzuje a presúva teplé vzduchové hmoty na pevninu, čím sa klíma na pobreží otepľuje.
736. Špecifické teplo hliníka je 920 J/kg °C. Čo to znamená?
To znamená, že na zahriatie 1 kg hliníka o 1 °C je potrebných 920 J.
737. Hliníkové a medené tyče rovnakej hmotnosti 1 kg sa ochladia o 1 °C. Koľko sa zmení vnútornej energie každý bar? Ktorá lišta sa zmení viac a o koľko?
738. Aké množstvo tepla je potrebné na zohriatie kilogramového železného predliatku o 45 °C?
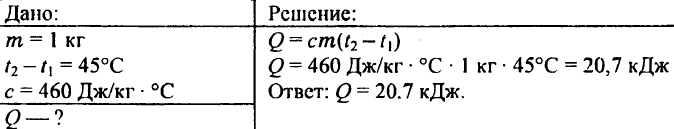
739. Koľko tepla je potrebné na zohriatie 0,25 kg vody z 30 °C na 50 °C?

740. Ako sa zmení vnútorná energia dvoch litrov vody pri zahriatí o 5 °C?

741. Koľko tepla je potrebné na zohriatie 5 g vody z 20 °C na 30 °C?
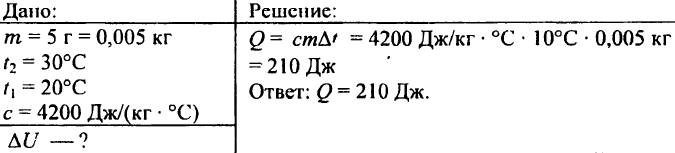
742. Aké množstvo tepla je potrebné na zahriatie hliníkovej gule s hmotnosťou 0,03 kg na 72 °C?
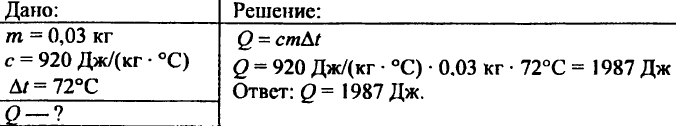
743. Vypočítajte množstvo tepla potrebného na zohriatie 15 kg medi o 80 °C.
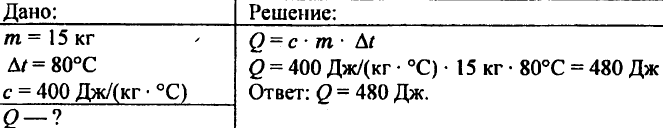
744. Vypočítajte množstvo tepla potrebného na zahriatie 5 kg medi z 10 °C na 200 °C.

745. Aké množstvo tepla je potrebné na zohriatie 0,2 kg vody z 15 °C na 20 °C?

746. Voda s hmotnosťou 0,3 kg sa ochladila o 20 °C. O koľko sa zníži vnútorná energia vody?

747. Koľko tepla je potrebné na zohriatie 0,4 kg vody s teplotou 20 °C na teplotu 30 °C?

748. Koľko tepla sa spotrebuje na ohrev 2,5 kg vody o 20 °C?
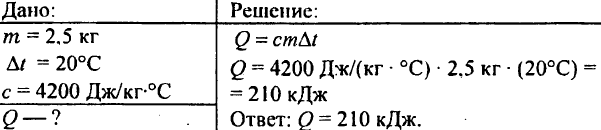
749. Koľko tepla sa uvoľnilo, keď sa 250 g vody ochladilo z 90 °C na 40 °C?

750. Aké množstvo tepla je potrebné na ohriatie 0,015 litra vody o 1 °C?

751. Vypočítajte množstvo tepla potrebného na ohrev jazierka s objemom 300 m3 o 10 °C?

752. Koľko tepla treba odovzdať 1 kg vody, aby sa jej teplota zvýšila z 30 °C na 40 °C?
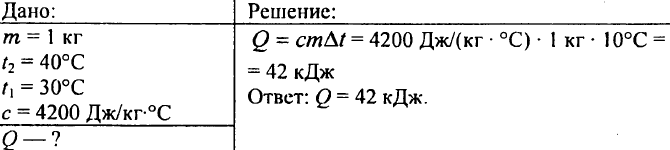
753. Voda s objemom 10 litrov sa ochladila z teploty 100 °C na teplotu 40 °C. Koľko tepla sa v tomto prípade uvoľní?

754. Vypočítajte množstvo tepla potrebného na zohriatie 1 m3 piesku o 60 °C.

755. Objem vzduchu 60 m3, merná tepelná kapacita 1000 J/kg °C, hustota vzduchu 1,29 kg/m3. Koľko tepla je potrebné na zvýšenie teploty na 22 °C?
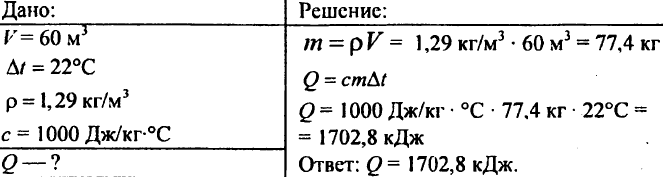
756. Voda sa ohriala o 10 °C, pričom sa spotrebovalo 4,20 103 J tepla. Určte množstvo vody.

757. Voda s hmotnosťou 0,5 kg vykázala 20,95 kJ tepla. Aká bola teplota vody, ak bola počiatočná teplota vody 20°C?
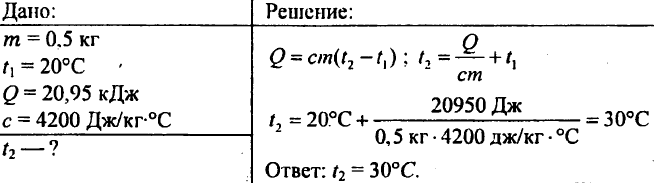
758. Do medeného hrnca s hmotnosťou 2,5 kg sa naleje 8 kg vody s teplotou 10 °C. Koľko tepla je potrebné na privedenie vody do varu v hrnci?

759. Liter vody s teplotou 15 °C sa naleje do medenej naberačky s hmotnosťou 300 g Koľko tepla je potrebné na zohriatie vody v naberačke o 85 °C?

760. Kus vyhriatej žuly s hmotnosťou 3 kg sa vloží do vody. Žula odovzdá vode 12,6 kJ tepla, chladenie o 10 °C. Aká je špecifická tepelná kapacita kameňa?
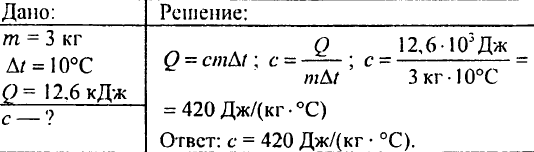
761. Horúca voda s teplotou 50 °C sa pridala k 5 kg vody s teplotou 12 °C, čím sa získala zmes s teplotou 30 °C. Koľko vody sa pridalo?

762. Voda s teplotou 20 °C sa pridala do 3 litrov vody s teplotou 60 °C, čím sa získala voda s teplotou 40 °C. Koľko vody sa pridalo?

763. Aká bude teplota zmesi, ak sa 600 g vody 80 °C zmieša s 200 g vody 20 °C?

764. Liter vody s teplotou 90 °C sa nalial do vody s teplotou 10 °C a teplota vody dosiahla 60 °C. Koľko bolo studená voda?
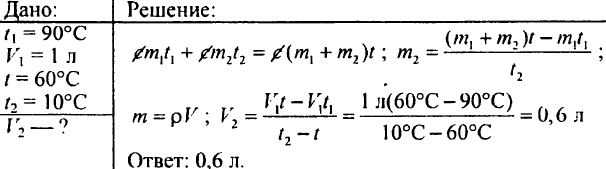
765. Určte, koľko horúcej vody zohriatej na 60°C treba naliať do nádoby, ak nádoba už obsahuje 20 litrov studenej vody s teplotou 15°C; teplota zmesi by mala byť 40 °C.
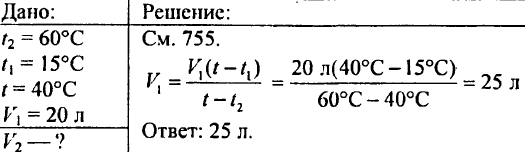
766. Určte, koľko tepla je potrebné na zohriatie 425 g vody o 20 °C.

767. O koľko stupňov sa ohreje 5 kg vody, ak voda prijme 167,2 kJ?

768. Koľko tepla je potrebné na zohriatie m gramov vody pri teplote t1 na teplotu t2?
769. 2 kg vody sa naleje do kalorimetra s teplotou 15 °C. Na akú teplotu sa zohreje voda v kalorimetri, ak sa do nej spustí mosadzné závažie s hmotnosťou 500 g zohriate na 100 °C? Špecifická tepelná kapacita mosadze je 0,37 kJ/(kg °C).

770. Sú tam kusy medi, cínu a hliníka rovnakého objemu. Ktorý z týchto kúskov má najväčšiu a ktorý najmenšiu tepelnú kapacitu?

771. Do kalorimetra sa nalialo 450 g vody, ktorej teplota je 20 °C. Keď sa do tejto vody ponorilo 200 g železných pilín zohriatych na 100 °C, teplota vody dosiahla 24 °C. Určte špecifickú tepelnú kapacitu pilín.

772. Medený kalorimeter s hmotnosťou 100 g pojme 738 g vody, ktorej teplota je 15 °C. Do tohto kalorimetra sa spustilo 200 g medi pri teplote 100 °C, potom teplota kalorimetra stúpla na 17 °C. Aká je špecifická tepelná kapacita medi?

773. Oceľová guľa s hmotnosťou 10 g sa vyberie z pece a spustí sa do vody s teplotou 10 °C. Teplota vody vystúpila na 25°C. Aká bola teplota gule v peci, ak hmotnosť vody bola 50 g? Merná tepelná kapacita ocele je 0,5 kJ/(kg °C).

777. 50 g vody s teplotou 19 °C sa naleje do vody s hmotnosťou 150 g s teplotou 35 °C. Aká je teplota zmesi?

778. Do liatinového kotla s hmotnosťou 2 kg sa pri teplote 10 °C naliala voda s hmotnosťou 5 kg s teplotou 90 °C. Aká bola teplota vody?

779. Oceľové dláto s hmotnosťou 2 kg sa zahrialo na teplotu 800 °C a potom sa spustilo do nádoby obsahujúcej 15 litrov vody s teplotou 10 °C. Na akú teplotu sa zohreje voda v nádobe?

(Indikácia. Na vyriešenie tohto problému je potrebné vytvoriť rovnicu, v ktorej sa požadovaná teplota vody v nádobe po spustení rezačky berie ako neznáma.)
780. Akú teplotu získa voda, ak zmiešate 0,02 kg vody s teplotou 15 °C, 0,03 kg vody s teplotou 25 °C a 0,01 kg vody s teplotou 60 °C?
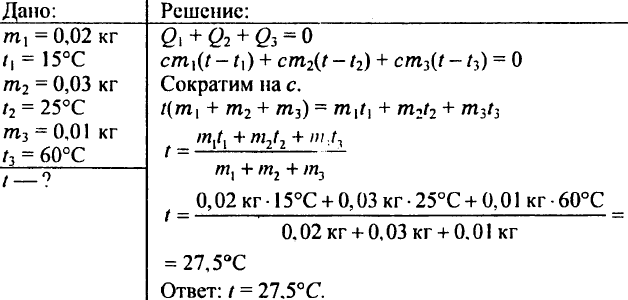
781. Vykurovanie dobre vetranej triedy si vyžaduje množstvo tepla 4,19 MJ za hodinu. Voda vstupuje do vykurovacích radiátorov s teplotou 80 °C a vystupuje s teplotou 72 °C. Koľko vody treba dodať do radiátorov každú hodinu?

782. Olovo s hmotnosťou 0,1 kg pri teplote 100 °C bolo ponorené do hliníkového kalorimetra s hmotnosťou 0,04 kg s obsahom 0,24 kg vody s teplotou 15 °C. Potom bola v kalorimetri nastavená teplota 16 °C. Aká je špecifická tepelná kapacita olova?

Keď hovoríme o spôsoboch vykurovania domu, možnostiach zníženia únikov tepla, musíme pochopiť, čo je teplo, v akých jednotkách sa meria, ako sa prenáša a ako sa stráca. Táto stránka poskytne základné informácie z kurzu fyziky potrebné na zváženie všetkých vyššie uvedených problémov.
Teplo je jedným zo spôsobov prenosu energie
Energia, ktorú telo prijíma alebo stráca v procese výmeny tepla s prostredím, sa nazýva množstvo tepla alebo jednoducho teplo.
V prísnom zmysle slova je teplo jedným zo spôsobov prenosu energie a iba množstvo energie prenesenej do systému má fyzikálny význam, ale slovo "teplo" je zahrnuté v takých osvedčených vedeckých pojmoch, ako je tepelný tok, tepelná kapacita , teplo fázového prechodu, teplo chemickej reakcie, tepelná vodivosť atď. Preto tam, kde používanie tohto slova nie je zavádzajúce, pojmy „teplo“ a „množstvo tepla“ sú synonymá. Tieto výrazy však možno použiť len vtedy, ak sú uvedené presná definícia, a v žiadnom prípade nemožno "množstvo tepla" pripísať počtu počiatočných konceptov, ktoré nevyžadujú definíciu. Aby sa predišlo chybám, pojem „teplo“ treba chápať práve ako spôsob prenosu energie a množstvo prenesenej energie týmto spôsobom označujeme pojmom „množstvo tepla“. Odporúča sa vyhnúť sa výrazu „tepelná energia“.
Teplo je kinetická časť vnútornej energie látky, určená intenzívnym chaotickým pohybom molekúl a atómov, ktoré tvoria túto látku. Teplota je mierou intenzity molekulárneho pohybu. Množstvo tepla, ktoré má teleso pri danej teplote, závisí od jeho hmotnosti; napríklad pri rovnakej teplote sa vo veľkej šálke vody nachádza viac tepla ako v malom a vo vedre studenej vody to môže byť viac ako v šálke horúcej vody (hoci teplota vody v vedro je nižšie).
Teplo je forma energie, a preto sa musí merať v jednotkách energie. AT medzinárodný systém Jednotkou energie SI je joule (J). Je tiež povolené používať mimosystémovú jednotku množstva tepla - kalórií: medzinárodná kalória je 4,1868 J.
Prenos tepla a prenos tepla
Prenos tepla je proces prenosu tepla v tele alebo z jedného telesa do druhého v dôsledku teplotných rozdielov. Intenzita prenosu tepla závisí od vlastností látky, teplotného rozdielu a riadi sa experimentálne stanovenými prírodnými zákonmi. Na vytvorenie efektívnych vykurovacích alebo chladiacich systémov, rôznych motorov, elektrární, tepelnoizolačných systémov potrebujete poznať princípy prenosu tepla. V niektorých prípadoch je prenos tepla nežiaduci (tepelná izolácia taviacich pecí, vesmírne lode atď.), kým v iných by mala byť čo najväčšia (parné kotly, výmenníky, kuchynské náčinie). Existujú tri hlavné typy prenosu tepla: vedenie, prúdenie a prenos tepla sálaním.
Tepelná vodivosť
Ak je vo vnútri telesa teplotný rozdiel, potom tepelná energia prechádza z jeho teplejšej časti do chladnejšej. Tento typ prenosu tepla v dôsledku tepelných pohybov a zrážok molekúl sa nazýva tepelná vodivosť. Tepelná vodivosť tyče sa odhaduje hodnotou tepelný tok, ktorý závisí od súčiniteľa tepelnej vodivosti, plochy prierezu, ktorým sa prenáša teplo a teplotného gradientu (pomer rozdielu teplôt na koncoch tyče k vzdialenosti medzi nimi). Jednotkou tepelného toku je watt.
TEPELNÁ VODIVOSŤ NIEKTORÝCH LÁTOK A MATERIÁLOV
Látky a materiály Tepelná vodivosť, W/(m^2*K)
Kovy
Hliník ____________________205
Bronz ______________________105
Volfrám ____________________159
Žehlička _____________________________________67
Meď _________________________389
Nikel _______________________58
Viesť _______________________35
Zinok _________________________113
Iné materiály
Azbest ________________________0,08
Betón _________________________0,59
Vzduch ________________________0,024
Eider down (voľne) ______0,008
Drevo (orech) _________________0,209
Piliny ________________________0,059
Guma (hubovitá) _____________0,038
Sklo ________________________0,75
Konvekcia
Konvekcia je prenos tepla v dôsledku pohybu hmôt vzduchu alebo kvapaliny. Pri pôsobení tepla na kvapalinu alebo plyn sa intenzita pohybu molekúl zvyšuje a v dôsledku toho sa zvyšuje tlak. Ak kvapalina alebo plyn nie sú obmedzené v objeme, potom expandujú; lokálna hustota kvapaliny (plynu) sa zmenšuje a v dôsledku vztlakových (archimedovských) síl sa ohriata časť média pohybuje nahor (preto teplý vzduch v miestnosti stúpa od batérií k stropu). V jednoduchých prípadoch prúdenia tekutiny potrubím alebo prúdenia okolo rovného povrchu možno koeficient konvekčného prestupu tepla vypočítať teoreticky. Doposiaľ sa však nepodarilo nájsť analytické riešenie problému konvekcie pre turbulentné prúdenie média.
tepelné žiarenie
Tretí typ prenosu tepla - prenos tepla sálaním - sa líši od vedenia tepla a konvekcie tým, že teplo sa v tomto prípade môže prenášať cez vákuum. Jeho podobnosť s inými spôsobmi prenosu tepla spočíva v tom, že je to spôsobené aj teplotným rozdielom. Tepelné žiarenie je jedným z typov elektromagnetického žiarenia.
Slnko je silným žiaričom tepelnej energie; ohrieva Zem aj na vzdialenosť 150 miliónov km. Intenzita slnečného žiarenia je približne 1,37 W/m2.
Rýchlosť prenosu tepla vedením a konvekciou je úmerná teplote a sálavý tepelný tok je úmerný štvrtej mocnine teploty.
Tepelná kapacita
Rôzne látky majú rôznu schopnosť akumulovať teplo; závisí to od ich molekulárnej štruktúry a hustoty. Množstvo tepla potrebné na zvýšenie teploty jednotkovej hmotnosti látky o jeden stupeň (1 ° C alebo 1 K) sa nazýva jej špecifická tepelná kapacita. Tepelná kapacita sa meria v J/(kg K).
Zvyčajne rozlišujte tepelnú kapacitu pri konštantnom objeme ( ŽIVOTOPIS) a tepelná kapacita pri konštantný tlak (C P), ak sa počas procesu zahrievania udržiava objem telesa alebo tlak konštantný, resp. Napríklad na zahriatie jedného gramu vzduchu v balóne o 1 K je potrebné viac tepla ako na jeho zohriatie rovnakým spôsobom v uzavretej nádobe s pevnými stenami, pretože časť energie odovzdanej balónu sa vynaloží na expanziu balónika. vzduchu, a nie jeho ohrevu. Keď sa zahrieva pri konštantnom tlaku, časť tepla ide na výrobu práce expanzie tela a časť - na zvýšenie jeho vnútornej energie, zatiaľ čo pri zahrievaní na konštantný objem sa všetko teplo vynakladá na zvýšenie vnútornej energie; týkajúci sa C R vždy viac ako ŽIVOTOPIS. Pre kvapaliny a tuhé látky je rozdiel medzi C R a ŽIVOTOPIS relatívne malé.
tepelné stroje
Tepelné motory sú zariadenia, ktoré premieňajú teplo na užitočná práca. Príkladmi takýchto strojov sú kompresory, turbíny, parné, benzínové a prúdové motory. Jedným z najznámejších tepelných motorov je parná turbína používaná v moderných tepelných elektrárňach. Zjednodušená schéma takejto elektrárne je na obrázku 1.

Ryža. 1. Zjednodušená schéma elektrárne s parnou turbínou pracujúcou na fosílne palivá.
Pracovná tekutina – voda – sa premieňa na prehriatu paru v parnom kotli vykurovanom spaľovaním fosílnych palív (uhlie, ropa alebo zemný plyn). Para vysoký tlak otáča hriadeľ parnej turbíny, ktorá poháňa generátor vyrábajúci elektrinu. Odpadová para sa pri ochladzovaní tečúcou vodou kondenzuje, ktorá absorbuje časť tepla. Ďalej sa voda privádza do chladiacej veže (chladiacej veže), odkiaľ sa časť tepla uvoľňuje do atmosféry. Kondenzát sa prečerpá späť do parného kotla a celý cyklus sa opakuje.
Ďalším príkladom tepelného motora je chladnička pre domácnosť, ktorej schéma je znázornená na obr. 2.

V chladničkách a domácich klimatizáciách sa energia dodáva zvonku, aby ju zabezpečila. Kompresor zvyšuje teplotu a tlak pracovnej látky chladničky - freónu, amoniaku alebo oxidu uhličitého. Prehriaty plyn sa privádza do kondenzátora, kde sa ochladzuje a kondenzuje a uvoľňuje teplo životné prostredie. Kvapalina opúšťajúca dýzy kondenzátora prechádza cez škrtiaci ventil do výparníka a časť sa odparí, čo je sprevádzané prudkým poklesom teploty. Výparník odoberá teplo z komory chladničky, ktorá ohrieva pracovnú tekutinu v dýzach; táto kvapalina je dodávaná kompresorom do kondenzátora a cyklus sa znova opakuje.
Vnútorná energia tela sa môže meniť v dôsledku práce vonkajších síl. Na charakterizáciu zmeny vnútornej energie pri prenose tepla sa zavádza veličina nazývaná množstvo tepla a označovaná Q.
V medzinárodnom systéme je jednotkou množstva tepla, ako aj práce a energie joule: = = = 1 J.
V praxi sa niekedy používa mimosystémová jednotka množstva tepla - kalória. 1 kal. = 4,2 J.
Treba si uvedomiť, že pojem „množstvo tepla“ je nešťastný. Bol zavedený v čase, keď sa verilo, že telá obsahujú nejakú beztiažovú, nepolapiteľnú tekutinu – kalorickú. Proces prenosu tepla údajne spočíva v tom, že kalorické, prelievajúce sa z jedného tela do druhého, nesie so sebou určité množstvo tepla. Teraz, keď poznáme základy molekulárno-kinetickej teórie štruktúry hmoty, chápeme, že v tele nie sú žiadne kalórie, mechanizmus zmeny vnútornej energie tela je iný. Sila tradície je však veľká a naďalej používame termín, zavedený na základe nesprávnych predstáv o povahe tepla. Zároveň by sme pri pochopení podstaty prenosu tepla nemali úplne ignorovať mylné predstavy o ňom. Naopak, nakreslením analógie medzi tokom tepla a tokom hypotetickej kalorickej kvapaliny, množstvom tepla a množstvom kalorií, je možné pri riešení niektorých tried problémov vizualizovať prebiehajúce procesy a správne riešiť problémy. Nakoniec sa na základe nesprávnych predstáv o kalorickom ako nosiči tepla naraz získali správne rovnice popisujúce procesy prenosu tepla.
Pozrime sa podrobnejšie na procesy, ktoré sa môžu vyskytnúť v dôsledku prenosu tepla.
Nalejte trochu vody do skúmavky a uzavrite ju zátkou. Skúmavku zaveste na tyč upevnenú na statíve a priveďte pod ňu otvorený plameň. Z plameňa skúmavka dostáva určité množstvo tepla a teplota kvapaliny v nej stúpa. Keď teplota stúpa, vnútorná energia kvapaliny sa zvyšuje. Dochádza k intenzívnemu procesu jeho odparovania. Expandujúce výpary kvapaliny vykonávajú mechanickú prácu, aby vytlačili zátku z trubice.
Urobme ďalší experiment s modelom dela vyrobeného z kusu mosadznej rúrky, ktorá je namontovaná na vozíku. Na jednej strane je rúrka tesne uzavretá ebonitovou zátkou, cez ktorú prechádza kolík. Drôty sú prispájkované k čapu a rúrke a končia na svorkách, ktoré môžu byť napájané zo siete osvetlenia. Model pištole je teda akýmsi elektrickým kotlom.
 |
Nalejte trochu vody do hlavne dela a uzavrite trubicu gumovou zátkou. Pripojte pištoľ k zdroju napájania. Elektrina, prechádzajúc vodou, ohrieva ju. Voda vrie, čo vedie k jej intenzívnemu odparovaniu. Zvyšuje sa tlak vodnej pary a nakoniec vytlačia korok z hlavne.
Pištoľ sa v dôsledku spätného rázu vráti späť v smere proti korku.
Obe skúsenosti spájajú nasledujúce okolnosti. V procese zahrievania kvapaliny rôznymi spôsobmi sa teplota kvapaliny a tým aj jej vnútorná energia zvýšila. Aby kvapalina vrela a intenzívne sa odparovala, bolo potrebné pokračovať v jej zahrievaní.
Pary kvapaliny vďaka svojej vnútornej energii vykonávali mechanickú prácu.
 |
Skúmame závislosť množstva tepla potrebného na zahriatie telesa od jeho hmotnosti, teplotných zmien a druhu látky. Na štúdium týchto závislostí použijeme vodu a olej. (Na meranie teploty v experimente sa používa elektrický teplomer, vyrobený z termočlánku spojeného so zrkadlovým galvanometrom. Jeden prechod termočlánku sa spustí do nádoby so studenou vodou, aby sa zabezpečila jeho konštantná teplota. Druhý prechod termočlánku meria teplotu skúmanej kvapaliny).
Zážitok pozostáva z troch sérií. V prvej sérii sa pre konštantnú hmotnosť konkrétnej kvapaliny (v našom prípade vody) študuje závislosť množstva tepla potrebného na jej ohrev od zmien teploty. Množstvo tepla prijatého kvapalinou z ohrievača (elektrického sporáka) sa bude posudzovať podľa doby ohrevu za predpokladu, že medzi nimi existuje priamo úmerný vzťah. Aby výsledok experimentu zodpovedal tomuto predpokladu, je potrebné zabezpečiť stály tok tepla z elektrického sporáka do vyhrievaného telesa. Na tento účel bol elektrický sporák vopred pripojený k sieti, takže na začiatku experimentu sa teplota jeho povrchu prestala meniť. Pre rovnomernejšie zahrievanie kvapaliny počas experimentu ju budeme miešať pomocou samotného termočlánku. Hodnoty teplomera budeme zaznamenávať v pravidelných intervaloch, až kým svetelná škvrna nedosiahne okraj stupnice.
Urobme záver: existuje priama úmernosť medzi množstvom tepla potrebného na zahriatie telesa a zmenou jeho teploty.
V druhej sérii experimentov budeme porovnávať množstvo tepla potrebného na zohriatie rovnakých kvapalín rôznej hmotnosti, keď sa ich teplota zmení o rovnakú hodnotu.
Pre uľahčenie porovnania získaných hodnôt sa hmotnosť vody pre druhý experiment odoberie dvakrát menej ako v prvom experimente.
Opäť budeme v pravidelných intervaloch zaznamenávať hodnoty teplomera.
Porovnaním výsledkov prvého a druhého experimentu môžeme vyvodiť nasledujúce závery.
V tretej sérii experimentov budeme porovnávať množstvá tepla potrebné na zahriatie rovnakých hmôt rôznych kvapalín, keď sa ich teplota zmení o rovnakú hodnotu.
Na elektrickom sporáku si rozohrejeme olej, ktorého hmotnosť sa rovná hmotnosti vody v prvom pokuse. Hodnoty teplomeru budeme zaznamenávať v pravidelných intervaloch.
Výsledok experimentu potvrdzuje záver, že množstvo tepla potrebné na zahriatie telesa je priamo úmerné zmene jeho teploty a navyše naznačuje závislosť tohto množstva tepla od druhu látky.
Keďže v experimente bol použitý olej, ktorého hustota je menšia ako hustota vody a na zahriatie oleja na určitú teplotu bolo potrebné menšie množstvo tepla ako na ohrev vody, možno predpokladať, že množstvo tepla potrebný na zahriatie telesa závisí od jeho hustoty.
Aby sme otestovali tento predpoklad, budeme súčasne ohrievať rovnaké masy vody, parafínu a medi na ohrievači s konštantným výkonom.
Po rovnakom čase je teplota medi asi 10-krát a parafín asi 2-krát vyššia ako teplota vody.
Ale meď má väčšiu a parafín menšiu hustotu ako voda.
Skúsenosti ukazujú, že veličina, ktorá charakterizuje rýchlosť zmeny teploty látok, z ktorých sú vyrobené telesá zapojené do výmeny tepla, nie je hustota. Táto veličina sa nazýva merná tepelná kapacita látky a označuje sa písmenom c.
 |
Na porovnanie špecifických tepelných kapacít rôzne látky je špeciálne zariadenie. Zariadenie pozostáva z regálov, v ktorých je pripevnená tenká parafínová doska a tyč s tyčami, ktoré cez ňu prechádzajú. Na koncoch tyčí sú vystužené hliníkové, oceľové a mosadzné valce rovnakú hmotnosť.
Na rovnakú teplotu ohrievame valce tak, že ich ponoríme do nádoby s vodou stojacej na rozpálenom elektrickom sporáku. Upevníme horúce valce na stojany a uvoľníme ich z upevňovacích prvkov. Valce sa súčasne dotýkajú parafínovej platne a po roztavení parafínu do nej začnú klesať. Hĺbka ponorenia valcov rovnakej hmotnosti do parafínovej platne, keď sa ich teplota zmení o rovnakú hodnotu, sa ukáže byť odlišná.
Skúsenosti ukazujú, že špecifické tepelné kapacity hliníka, ocele a mosadze sú rôzne.
Po vykonaní zodpovedajúcich experimentov s tavením pevné látky, odparovanie kvapalín, spaľovanie paliva, získavame nasledovné kvantitatívne závislosti.
Na získanie jednotiek špecifických veličín je potrebné ich vyjadriť z príslušných vzorcov a do výsledných výrazov nahradiť jednotky tepla - 1 J, hmotnosti - 1 kg a pre špecifické teplo - 1 K.
Získame jednotky: merná tepelná kapacita - 1 J / kg K, ostatné merné teplo: 1 J / kg.
Učebný cieľ: Oboznámiť sa s pojmami množstvo tepla a merná tepelná kapacita.
Rozvojový cieľ: Kultivovať všímavosť; naučiť sa myslieť, robiť závery.
1. Aktualizácia témy
2. Vysvetlenie nového materiálu. 50 min.
Už viete, že vnútorná energia tela sa môže meniť vykonávaním práce aj odovzdávaním tepla (bez vykonávania práce).
Energia, ktorú telo prijme alebo stratí pri prenose tepla, sa nazýva množstvo tepla. (zápis do notebooku)
To znamená, že jednotkami merania množstva tepla sú tiež Jouly ( J).
Uskutočňujeme experiment: dve poháre v jednom 300 g vody a v druhom 150 g a železný valec s hmotnosťou 150 g Obe poháre sú umiestnené na rovnakej dlaždici. Po určitom čase teplomery ukážu, že voda v nádobe, v ktorej sa telo nachádza, sa ohrieva rýchlejšie.
To znamená, že na ohrev 150 g železa je potrebné menej tepla ako na ohrev 150 g vody.
Množstvo tepla preneseného do tela závisí od druhu látky, z ktorej je telo vyrobené. (zápis do notebooku)
Navrhujeme otázku: je rovnaké množstvo tepla potrebné na zahriatie telesa rovnakej teploty, ktoré však pozostávajú z rôzne látky?
Vykonávame experiment so zariadením Tyndall na určenie špecifickej tepelnej kapacity.
Dospeli sme k záveru: telesá z rôznych látok, ale rovnakej hmotnosti, sa pri ochladzovaní uvoľňujú a vyžadujú pri zahriatí o rovnaký počet stupňov iná suma teplo.
Robíme závery:
1. Na zahriatie telies rovnakej hmotnosti, pozostávajúcich z rôznych látok, na rovnakú teplotu je potrebné iné množstvo tepla.
2. Telesá rovnakej hmotnosti, pozostávajúce z rôznych látok a zahriate na rovnakú teplotu. Pri ochladení o rovnaký počet stupňov vydávajú iné množstvo tepla.
Robíme záver, že množstvo tepla potrebné na zvýšenie jedného stupňa jednotkovej hmotnosti rôznych látok bude rôzne.
Uvádzame definíciu mernej tepelnej kapacity.
Fyzikálna veličina, ktorá sa číselne rovná množstvu tepla, ktoré sa musí odovzdať telesu s hmotnosťou 1 kg, aby sa jeho teplota zmenila o 1 stupeň, sa nazýva merné teplo látky.
Zavádzame jednotku merania mernej tepelnej kapacity: 1J / kg * stupeň.
Fyzický význam tohto pojmu : merná tepelná kapacita ukazuje, ako veľmi sa zmení vnútorná energia 1 g (kg.) látky pri jej zahriatí alebo ochladení o 1 stupeň.
Zvážte tabuľku špecifických tepelných kapacít niektorých látok.
Problém riešime analyticky
Koľko tepla je potrebné na zahriatie pohára vody (200 g) z 20 0 na 70 0 C.
Na ohrev 1 g na 1 g. Potrebné - 4,2 J.
A na zahriatie 200 g na 1 g to bude trvať ďalších 200 - 200 * 4,2 J.
A na zahriatie 200 g o (70 0 - 20 0) to bude trvať ďalších (70 - 20) viac - 200 * (70 - 20) * 4,2 J
Nahradením údajov dostaneme Q = 200 * 50 * 4,2 J = 42 000 J.
Výsledný vzorec zapíšeme v zmysle zodpovedajúcich veličín
4. Čo určuje množstvo tepla prijatého telesom pri zahrievaní?
Upozorňujeme, že množstvo tepla potrebného na zahriatie telesa je úmerné hmotnosti telesa a zmene jeho teploty.,
Existujú dva valce rovnakej hmotnosti: železné a mosadzné. Je potrebné rovnaké množstvo tepla na ich zahriatie o rovnaký počet stupňov? prečo?
Koľko tepla je potrebné na zohriatie 250 g vody z 20 na 60 0 C.
Aký je vzťah medzi kalóriami a joulmi?
Kalória je množstvo tepla potrebné na zvýšenie teploty 1 gramu vody o 1 stupeň.
1 kal = 4,19 = 4,2 J
1 kcal = 1 000 kcal
1 kcal=4190J=4200J
3. Riešenie problémov. 28 min.
Ak sa valce z olova, cínu a ocele vyhrievané vo vriacej vode s hmotnosťou 1 kg položia na ľad, ochladia sa a časť ľadu pod nimi sa roztopí. Ako sa zmení vnútorná energia valcov? Pod ktorým z valcov sa bude topiť viac ľadu, pod ktorým - menej?
Vyhrievaný kameň s hmotnosťou 5 kg. Ochladením vo vode o 1 stupeň jej odovzdá 2,1 kJ energie. Aká je špecifická tepelná kapacita kameňa
Pri kalení sekáč sa najskôr zahrial na 650 0, potom sa spustil do oleja, kde sa ochladil na 50 0 C. Aké množstvo tepla sa uvoľnilo, ak jeho hmotnosť bola 500 g.
Koľko tepla sa vynaložilo na ohrev z 20 0 na 1220 0 C. oceľový predvalok pre kľukový hriadeľ kompresora s hmotnosťou 35 kg.
Samostatná práca
Aký druh prenosu tepla?
Žiaci dopĺňajú tabuľku.
- Vzduch v miestnosti sa ohrieva cez steny.
- Cez otvorené okno, ktorý zahŕňa teplý vzduch.
- Cez sklo, ktoré prepúšťa slnečné lúče.
- Zem sa zahrieva lúčmi slnka.
- Kvapalina sa zahrieva na sporáku.
- Oceľová lyžička sa zahrieva čajom.
- Vzduch je ohrievaný sviečkou.
- Plyn sa pohybuje okolo častí stroja produkujúcich teplo.
- Vyhrievanie hlavne guľometu.
- Varenie mlieka.
5. Domáca úloha: Peryshkin A.V. „Fyzika 8“ §§ 7, 8; zbierka úloh 7-8 Lukashik V.I. č. 778-780, 792,793 2 min.
Koncept množstva tepla vznikol na skoré štádia rozvoj modernej fyziky, keď ešte neexistovali jasné predstavy o vnútorná štruktúra hmote, o tom, čo je energia, o tom, aké formy energie existujú v prírode a o energii ako forme pohybu a premeny hmoty.
Množstvo tepla je fyzikálne množstvo ekvivalent energie odovzdanej hmotnému telu v procese výmeny tepla.
Zastaranou jednotkou množstva tepla je kalória, rovná sa 4,2 J, dnes sa táto jednotka prakticky nepoužíva a jej miesto zaujal joule.
Spočiatku sa predpokladalo, že nosičom tepelnej energie je nejaké úplne beztiažové médium, ktoré má vlastnosti kvapaliny. Na základe tohto predpokladu sa riešili a stále riešia mnohé fyzikálne problémy prenosu tepla. Existencia hypotetickej kalórie bola braná ako základ mnohých v podstate správnych konštrukcií. Verilo sa, že kalorické látky sa uvoľňujú a absorbujú pri fenoméne zahrievania a chladenia, topenia a kryštalizácie. Správne rovnice pre procesy prenosu tepla boli získané z nesprávnych fyzikálnych konceptov. Existuje známy zákon, podľa ktorého je množstvo tepla priamo úmerné hmotnosti telesa zapojeného do výmeny tepla a teplotnému gradientu:
Kde Q je množstvo tepla, m je hmotnosť telesa a koeficient s- veličina nazývaná merná tepelná kapacita. Špecifická tepelná kapacita je charakteristická pre látku zapojenú do procesu.
Práca v termodynamike
V dôsledku tepelných procesov, čisto mechanická práca. Napríklad plyn pri zahrievaní zväčšuje svoj objem. Zoberme si situáciu ako na obrázku nižšie:

V tomto prípade sa mechanická práca bude rovnať sile tlaku plynu na piest vynásobenej dráhou, ktorú prejde piest pod tlakom. Samozrejme, toto je ten najjednoduchší prípad. Ale aj v ňom možno zaznamenať jednu ťažkosť: tlaková sila bude závisieť od objemu plynu, čo znamená, že nemáme do činenia s konštantami, ale s premennými. Keďže všetky tri premenné: tlak, teplota a objem spolu súvisia, výpočet práce sa stáva oveľa komplikovanejším. Existuje niekoľko ideálnych, nekonečne pomalých procesov: izobarické, izotermické, adiabatické a izochorické - pre ktoré sa takéto výpočty dajú vykonať relatívne jednoducho. Vynesie sa graf závislosti tlaku na objeme a práca sa vypočíta ako integrál tvaru.
